4518 molecole, già approvate dalle autorità per il trattamento di patologie come diabete, artrite, infiammazione e alcolismo, o semplicemente note per essere attive su specifici target cellulari, sono state testate su 578 linee cellulari tumorali umane. Il risultato è stato davvero straordinario: circa 50 di queste molecole sono risultate attive come antitumorali. Questa ricerca potrebbe portare, in tempi rapidi, ad un riposizionamento di questi farmaci per il trattamento di diversi tumori. Ma lo studio ha consentito anche di individuare nuovi target cellulari, utili allo sviluppo di nuove classi di anticancro.
Screening 'a strascico' di nuovi antitumorali
La strategia dei ricercatori del Broad Institute of MIT and Harvard e del Dana-Farber Cancer Institute è concettualmente molto semplice. Prendere migliaia di farmaci già approvati, ed impiegati per il trattamento di varie patologie non-oncologiche (ma anche oncologiche), e andarle a studiare su un panel molto ampio di linee cellulari tumorali umane. Se alcuni di questi farmaci dovessero risultare attivi, si potrebbe saltare tutta la fase sulla sicurezza e tollerabilità clinica del farmaco.
Si tratterebbe del classico riposizionamento di un farmaco approvato inizialmente per una indicazione e poi, in una fase successiva, anche per altre indicazioni terapeutiche.
Solo che in passato, i pochi esempi di questo tipo, in oncologia, sono arrivati per caso. Ora, il lavoro pubblicato su Nature Cancer, come primo autore Steven M. Corsello, oncologo di Dana-Farber, descrive un approccio sistematico e su vasta scala. Ecco alcuni dettagli.
Oltre 6.000 farmaci (intera farmacopea), già approvati dalla FDA - o comunque noti per essere attivi per alcune indicazioni terapeutiche e ben tollerati - rappresentano il numero potenziale di molecole da poter testare su 578 linee cellulari tumorali umane, un numero senza precedenti che copre 24 tipi di tumore.
Finora sono stati testati 4.518 farmaci, e di questi solo alcuni già noti come anticancro.
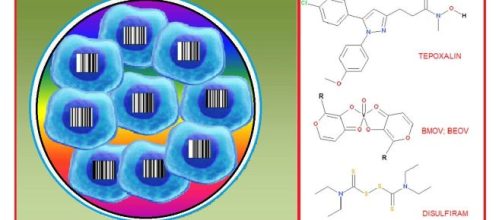
La tecnica sfruttata per questo screening è stata PRISM (profiling relative inhibition simultaneously in mixtures), un metodo che permette di etichettare (tipo codice a barre) moltissime linee cellulari e di poterle testare in miscela, senza la necessità di ripetere lo stesso test su ognuna di esse.
Grazie a questa tecnica, migliaia di molecole sono state testate in tempi relativamente brevi su tutte le linee cellulari tumorali. Ogni farmaco testato è stato prima analizzato per la sua conformità e purezza, mediante tecniche LC/MS. Il risultato è stato davvero sorprendente: molti farmaci non-oncologici sono risultati attivi su diversi tumori.
Alcuni risultati straordinari
Dei 4.518 farmaci finora testati, 3.350 (74%) sono già approvati o in fase di sviluppo clinico, negli Stati Uniti o in Europa. I restanti 1.168 (26%) sono composti di riferimento ad attività nota. La maggior parte dei composti, 3.466 (77%) non aveva un profilo oncologico noto, i restanti composti erano chemioterapici (2%) o agenti oncologici mirati (21%).
Lo screening è stato suddiviso in due fasi, nella prima tutti i prodotti sono stati studiati ad un singolo dosaggio (2,5 µM). I composti attivi, ben 1.448 farmaci di cui 774 (53%) non-oncologici, sono passati alla seconda fase, facendo una dose-risposta (10 µM - 610 pM).
Lo studio PRISM ha permesso, ad esempio, di selezionare alcune molecole citotossiche il cui meccanismo è basato sulla stabilizzazione dell’interazione PDE3A-SLFN12, come anagrelide e zardaverina, noti inibitori PDE3A (fosfodiesterasi 3A); tanaproget, un agonista dei recettori progestinici; AG-1296, inibitore di alcune chinasi e di PDGFR; DCEBIO, un attivatore del canale del potassio. La proteina SLFN12 (Schlafen 12) si lega ai ribosomi e ne regola l’attività.
Sebbene i composti individuati, capaci di stabilizzare queste due proteine, siano poco potenti, questa scoperta sarà la base per i chimici farmaceutici nel progettare nuovi antitumorali.
Tre esempi eloquenti
Il Disulfiram è un inibitore dell’acetaldeide deidrogenasi utilizzato nel trattamento degli alcolisti. Con questo farmaco chi beve alcool accumula acetaldeide nell’organismo che genera spiacevoli effetti come palpitazione, cefalea e vomito. Effetti che dissuadono l’alcolista dal continuare a bere alcolici. Questo farmaco è risultato citotossico su alcune linee tumorali attraverso un meccanismo associato alla regolazione di due metallotioneine (MT1E ed MT2A), antiossidanti non-enzimatici delle cellule.
Le metallotioneine chelano il rame, come fa anche disulfiram. Questo farmaco potrebbe essere indicato per i tumori al seno e alle ovaie.
Il BMOV (Bis(maltolato)-oxovanadio (IV) e il BEOV (Bis(etilmaltolato)-ossovanadio (IV) sono due farmaci sperimentali antidiabetici, a base di vanadio, che regolano l'espressione del trasportatore di solfato SLC26A2. Alcuni tumori, come il melanoma e i tumori uterini, over-esprimono SLC26A2. BMOV e BEOV potrebbero essere indicati in questi tumori.
La Tepossalina è un antiinfiammatorio veterinario, inibitore di cicloossigenasi (COX) e lipossigenasi (LOS), approvato dalla FDA nell’osteoartrosi dei cani. La cosa sorprendente è stata che, contrariamente ad altri farmaci antitumorali, come taxani (docetaxel e paclitaxel), vinca alcaloidi (vincristina e vinorelbina) e inibitori del proteasoma (carfilzomib), che diventano inefficaci quando aumenta l’espressione del trasportatore ABCB1 alla base della farmaco-resistenza, la tepossalina invece aumenta la sua attività antitumorale.
Ma non è chiaro esattamente con quale meccanismo.
Todd Golub, Direttore del Cancer Program e uno degli autori dello studio, ha dichiarato: “Prima di iniziare, pensavamo che saremmo stati fortunati se avessimo trovato anche un singolo composto con proprietà anticancro. Siamo rimasti molto sorpresi di averne trovati così tanti”.