Grazie ad un algoritmo di apprendimento automatico (intelligenza artificiale), i ricercatori del MIT (Istituto di Tecnologia del Massachusetts) sono riusciti a identificare l'alicina, un nuovo potente antibiotico efficace nel distruggere molti ceppi batterici resistenti agli antibiotici attualmente disponibili. Un fenomeno allarmante quello della "multidrug resistance" all'attenzione della OMS che, se non si trovano subito delle soluzioni, potrà rappresentare una delle principali criticità di salute pubblica dei prossimi anni.
Un antidiabetico ad attività antibatterica
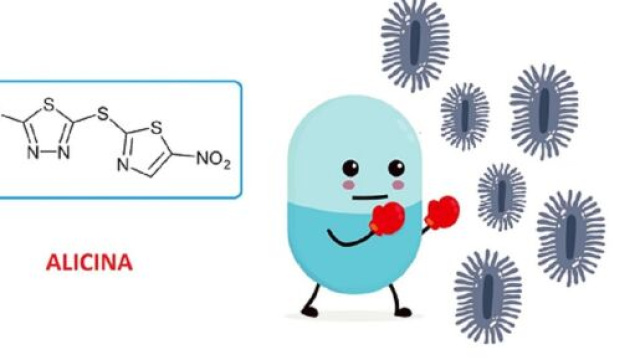
L’intelligenza artificiale è l’ultima frontiera nello sviluppo dei nuovi farmaci. Sia nel “drug-repositioning”, ovvero nell'impiego di vecchi farmaci per nuove indicazioni, che nello sviluppo di nuove molecole. Grazie a degli algoritmi, i ricercatori del Massachusetts Institute of Technology (MIT), una università privata di Cambridge, nel Massachusetts, hanno identificato l'alicina (SU-3327), una molecola già nota.
A questo risultato si è giunti progettando un modello virtuale in grado di selezionare composti con strutture chimiche ritenute efficaci nell'uccidere l’Escherichia coli. Per fare ciò, hanno "addestrato" il modello su circa 2.500 molecole, tra cui circa 1.700 farmaci approvati dalla FDA e 800 prodotti naturali con diverse strutture e una vasta gamma di attività biologiche.
Alla fine hanno identificato l’alicina, un composto noto sviluppato come antidiabetico ma mai approvato.
Si tratta di un inibitore di una chinasi, l’enzima JNK (c-Jun N-terminal kinase). Si è rivelato un potente antibiotico ad ampio spettro. Testato in vivo, su animali di laboratorio, l’alicina è risultata efficace su ceppi di batteri resistenti ai comuni antibiotici, come il Clostridium difficile (normalmente presente nell'intestino ma che, dopo una terapia antibiotica, può dare gravi forme di diarrea e disturbi gastro-intestinali), l’Acinetobacter baumannii (batterio che ha infettato molti soldati statunitensi di stanza in Iraq e in Afghanistan) e il Mycobacterium tuberculosis (che causa tubercolosi).
L’unico ceppo dove questo farmaco non ha funzionato è stato lo Pseudomonas aeruginosa, un patogeno polmonare difficile da trattare.
La cosa più interessante di questo risultato è il meccanismo di azione. Quest’antibiotico è un “sideroforo” ovvero una molecola che sottrae ioni ferro dalle cellule batteriche, alterando l’equilibrio elettrochimico intorno alla membrana batterica. Un meccanismo differente dagli altri antibiotici e per questo efficace anche sui ceppi resistenti.
Una nuova era nella scoperta degli antibiotici
Negli ultimi decenni, sono stati sviluppati pochissimi nuovi antibiotici e quelli recentemente approvati agiscono con meccanismi simili ai “vecchi” antibiotici. Lo sviluppo di un nuovo antibiotico richiede enormi investimenti, tante prove sperimentali e molti anni.
E, nonostante questo, le strutture chimiche non si distanziano molto da quelle degli antibiotici già disponibili in commercio con il risultato che, anche se nuovi, ben presto risultano inefficaci verso i ceppi batterici multi-resistenti.
"Volevamo sviluppare una piattaforma che ci consentisse di sfruttare il potere dell'intelligenza artificiale per inaugurare una nuova era per la scoperta di farmaci antibiotici", ha dichiarato James Collins, professore di ingegneria medica e scienze presso l'Istituto di ingegneria e scienza del MIT (IMES) e Dipartimento di Ingegneria Biologica. "Il nostro approccio ha permesso di selezionare questa straordinaria molecola che è probabilmente uno degli antibiotici più potenti finora scoperti".
Questo modello computerizzato, in pochi giorni, è in grado di vagliare più di cento milioni di composti chimici. È stato programmato per identificare potenziali antibiotici ad attività battericida, attivi con meccanismi diversi dagli antibiotici attualmente disponibili.
Oltre all'alicina, la piattaforma ha identificato altri potenziali antibiotici che, a breve, verranno testati in laboratorio. Inoltre, questa tecnologia non solo consente di selezionare molecole già note (“drug-repositioning”) ma potrà essere sfruttata per progettare nuovi farmaci, capitalizzando le informazioni acquisite nella selezione delle molecole note, poi risultate attive nelle prove di laboratorio.
"Il modello di apprendimento automatico consente di esplorare, in silico, ampi spazi chimici che possono essere proibitivi in termini di costi attraverso gli approcci sperimentali tradizionali", afferma Regina Barzilay, professore Delta Electronics di ingegneria elettrica e informatica nel laboratorio di informatica e intelligenza artificiale del MIT (CSAIL). Il 20 febbraio questa ricerca è stata pubblicata su Cell, primo autore Jonathan M. Stokes, postdoc presso il MIT e il Broad Institute of MIT e Harvard.