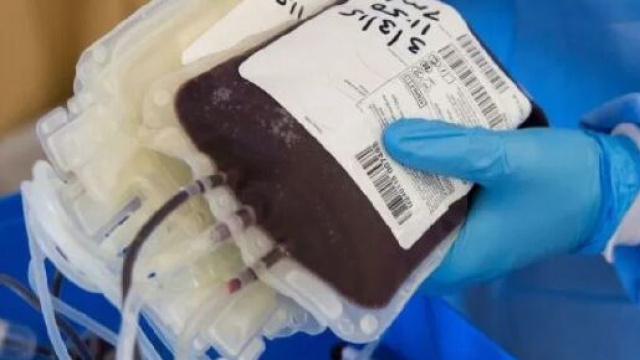
Poter usare il plasma dei soggetti che sono guariti dal Covid-19 e che, si ipotizza, siano ricchi di anticorpi anti-coronavirus, è un approccio noto da un secolo. È stato appena pubblicato un lavoro (PNAS) sulla trasfusione di plasma su 10 pazienti in Cina. Ma ora è necessario stabilire delle Linee Guida per il Covid-19, valide per tutti. Negli ultimi giorni sia Food and Drug Administration (FDA) che Commissione europea (CE) hanno pubblicato delle Linee Guida su questa procedura. Ai ricercatori ed operatori sanitari, vengono indicate le raccomandazioni su gestione, trattamento e indicazioni cliniche da seguire per ogni singolo paziente.
E sui criteri di selezione dei pazienti candidabili a questo trattamento.
Pratica nota da cent’anni
In presenza di una pandemia da infezione virale, come quella attuale da Covid-19, molte persone guariscono o superano la malattia senza la necessità di terapie e vaccini. Questo grazie ad una reazione del loro sistema immunitario che sviluppa una immunità con la produzione di anticorpi specifici contro l’attacco virale.
Poter usare il plasma di questi soggetti, ricco di questo anticorpi, per trattare altri pazienti che stanno lottando contro la malattia, rappresenta un approccio noto da molti anni, e che la stessa OMS (Organizzazione Mondiale della Sanità) considera praticabile. Il plasma può essere trasfuso tal quale oppure può essere usato per estrarre solo le immunoglobuline (anticorpi) in esso presenti.
Questa procedura è stata già seguita in passato per far fronte ad altre epidemie come quella della SARS-CoV del 2003, della pandemia da virus influenzale H1N1 del 2009-2010 e nell’epidemia MERS-CoV del 2012. Anche nel caso dell’attuale SARS-CoV-2, in attesa di un vaccino o di terapie efficaci, l’OMS vuole valutare l’efficacia di questo approccio.
Pubblicato su PNAS
Finora non ci sono dati a sufficienza per poter suggerire agli operatori sanitari un preciso protocollo da seguire. Per questo è necessario dare delle indicazioni precise agli operatori, in modo da poter poi raccogliere tutti i dati generati e stabilire le migliori condizioni da seguire.
A tal fine, negli ultimi giorni sia la Food and Drug Administration (FDA) che la Commissione europea (CE) hanno pubblicato delle Linee Guida su questa procedura.
Questo a beneficio dei ricercatori e degli operatori sanitari, fornendo loro raccomandazioni sulla gestione, il trattamento e lo studio del plasma nella pratica clinica, per ogni singolo paziente. Forniscono inoltre istruzioni sui criteri di ammissibilità dei pazienti e sulla modalità della raccolta del plasma. Prevedendo anche un monitoraggio con studi osservazionali condotti in parallelo, verso gruppi placebo.
A Wuhan, dove sono stati segnalati i primi casi di questa pandemia, i medici hanno già effettuato la trasfusione di plasma da soggetti guariti a soggetti malati. Lo studio, da poco pubblicato su PNAS, primo nome Kai Duan, ha coinvolto 10 pazienti gravi (diagnosi confermata dal test dell’RNA virale) a cui sono stati somministrati 200 ml di plasma prelevati da soggetti guariti.
In aggiunta ad una terapia antivirale.
Quello che è stato osservato è un rapido aumento degli anticorpi (1:640), un aumento dell’ossigenazione del sangue già dopo 3 giorni, e una diminuzione della proteina C-reattiva (18,13 mg / L contro 55,98 mg / L). Il recupero è stato più rapido così come la valutazione oggettiva mediante esame radiologico, con lesioni riassorbite entro 7 giorni.
Le Linee Guida
Queste linee guida non sono formalmente vincolanti ma, se seguite, i risultati ottenuti possono aiutare la comunità scientifica. In Europa, le Linee Guida sono state sviluppate in collaborazione con il Centro europeo per la prevenzione e il controllo delle malattie (ECDC), e sono state approvate dalle autorità competenti dei 27 Stati membri.
European Blood Alliance (EBA) e Direzione Generale dell'Informatica della Commissione europea (DG DIGIT) stanno elaborando un database dove verranno raccolti i dati sui donatori e i risultati ottenuti sui pazienti trattati. Questa banca dati, a libero accesso, potrà fornire a tutti gli interessati – ricercatori, operatori sanitari, autorità istituzionali – una indicazione concreta sull’efficienza di questa pratica.
Le Linee Guida statunitense, stabilite dalla Food and Drug Administration (FDA), prevedono l’uso delle trasfusioni di plasma da soggetto guarito ma solo dopo purificazione del sangue, e a pazienti COVID-19 di età pari o superiore a 18 anni, ricoverati in terapia intensiva e con una grave insufficienza respiratoria.
La necessità di purificare il sangue del donatore, da una serie di piccole proteine (mediatori infiammatori) che si possono sviluppare con la tempesta infiammatoria durante l’infezione, è ritenuta una pratica utile per scongiurare, nel soggetto ricevente, eventuali gravi infiammazioni, shock, insufficienza respiratoria, insufficienza d'organo e morte.